2010版gmp实施指南-水系统
时间:2024-11-17 来源:网络 人气:
2010版GMP实施指南——水系统解析

随着药品生产质量管理规范(GMP)的不断完善和更新,2010版GMP的实施指南为我国药品生产企业提供了更为详细和具体的要求。本文将重点解析2010版GMP实施指南中的水系统部分,以帮助企业和相关人员更好地理解和执行相关规范。
一、水系统概述

水系统是药品生产过程中不可或缺的一部分,其质量直接影响到药品的安全性、有效性和稳定性。2010版GMP实施指南对水系统的要求主要包括以下几个方面:
二、水质要求

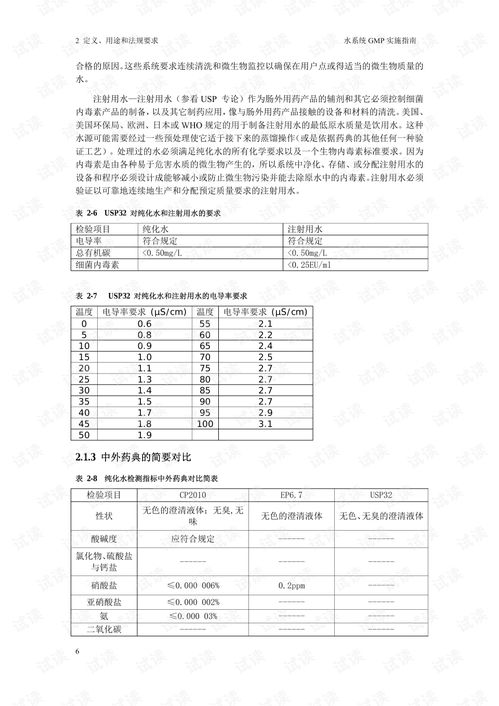
1. 水质标准:2010版GMP实施指南要求,制药用水必须符合《中华人民共和国药典》2010年版的规定,并满足以下要求:
(1)纯化水:电阻率大于0.5 M·cm,符合药典规定。
(2)注射用水:符合药典规定,用于注射剂、眼用制剂、输液剂等。
(3)灭菌注射用水:符合药典规定,用于注射剂、眼用制剂、输液剂等。
三、水系统设计

1. 设计原则:水系统设计应遵循以下原则:
(1)确保水质符合规定标准。
(2)防止交叉污染。
(3)便于操作和维护。
(4)节约能源。
四、水系统设施与设备
1. 原水处理:原水处理设施包括原水水箱、原水增压泵、多介质过滤器、活性炭过滤器等,用于去除原水中的悬浮物、胶体、有机物等。
2. 纯化水制备:纯化水制备设施包括反渗透装置、离子交换装置、超滤装置等,用于制备符合药典规定的水质。
3. 注射用水制备:注射用水制备设施包括蒸馏装置、纯化水循环系统、无菌空气系统等,用于制备符合药典规定的注射用水。
4. 灭菌注射用水制备:灭菌注射用水制备设施包括蒸馏装置、纯化水循环系统、无菌空气系统、无菌过滤系统等,用于制备符合药典规定的灭菌注射用水。
五、水系统运行与维护

1. 运行管理:水系统运行应遵循以下要求:
(1)定期监测水质,确保符合规定标准。
(2)定期检查设备,确保设备正常运行。
(3)定期清洗、消毒设备,防止交叉污染。
(4)记录运行数据,便于追溯和改进。
2010版GMP实施指南对水系统的要求较为严格,企业和相关人员应充分了解和掌握相关规范,确保水系统的正常运行,为药品生产提供优质的水源。同时,企业和相关人员还应不断学习和改进,提高水系统的管理水平,为我国药品生产质量提供有力保障。
教程资讯
教程资讯排行